Sincrotró ALBA
Els metalofàrmacs basats en iridi estan emergint com a noves eines per destruir cèl·lules canceroses desajustant el balanç redox intracel·lular. Científics del Sincrotró ALBA, IMDEA Nanociencia, ESRF i CNB-CSIC, han correlacionat en la mateixa cèl·lula, per primera vegada, dues tècniques d'imatge 3D de raigs-X per observar en acció un agent anticancerós al nano-espai intracel·lular d'una cèl·lula crio-preservada.

Dades reals on es mostra una secció 3D d'una cèl·lula de càncer de mama crio-preservada. La paleta de colors que varia del lila al groc indica la densitat d'iridi i els mitocondris es mostren com una malla groga. L'iridi s'observa exclusivament a l'interior dels mitocondris. També hi són presents altres orgànuls: el nucli en blau, vesícules denses en vermell, gotes lipídiques en verd i vacúols en blanc.
Els quimioterapèutics són fonamentals a la clínica per lluitar contra la majoria de càncers, i els nous fàrmacs ofereixen la possibilitat de facilitar interaccions intracel·lulars noves i singulars que modulin la maquinària cel·lular per així destruir la cèl·lula cancerosa. De la mateixa manera, són necessàries noves eines que facin possible la localització i quantificació d’aquestes molècules en el nano-espai intracel·lular per poder entendre del tot la seva acció terapèutica.
Investigadors de IMDEA Nanociencia, el Sincrotró ALBA, el Sincrotró Europeu de Grenoble (ESRF) i el Centre Nacional de Biotecnologia (CNB) han desenvolupat una nova família de candidats a fàrmac d'organo-iridi cent vegades més actius que el medicament cisplatí, utilitzat actualment a la clínica.
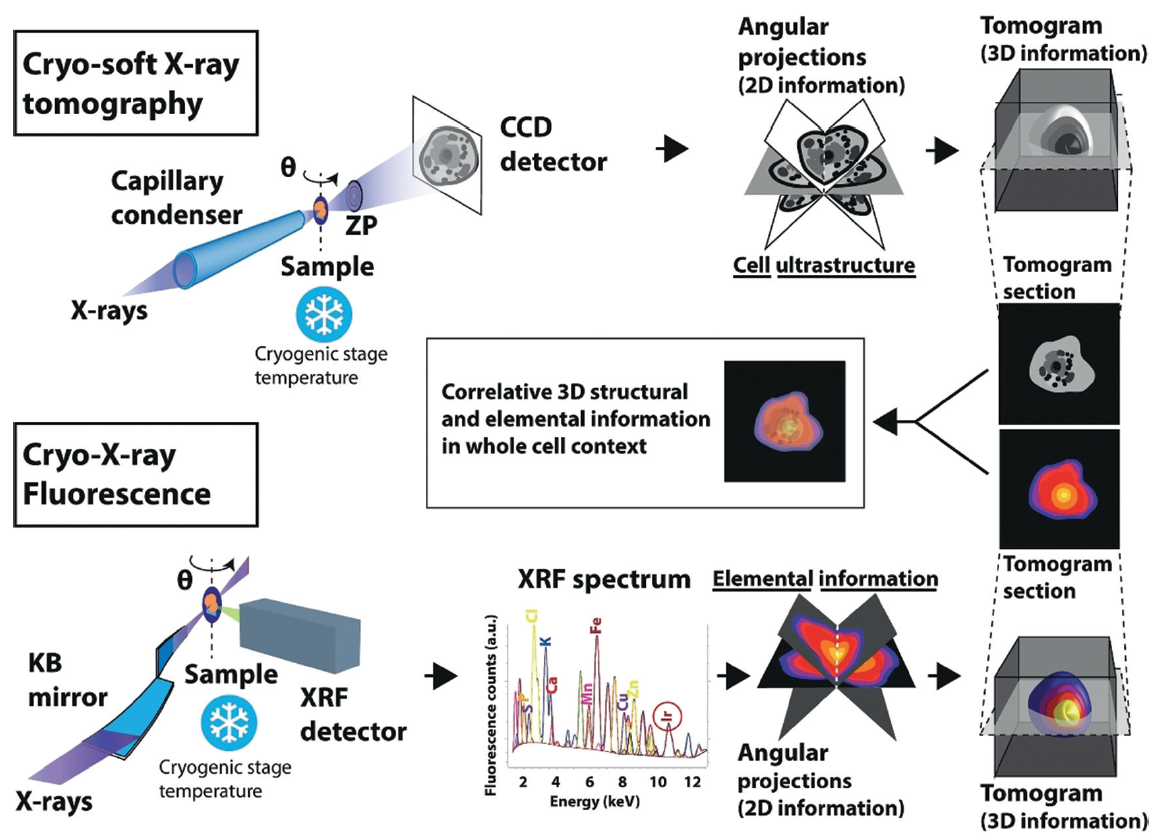
Per entendre el potencial terapèutic d'un compost, és crucial localitzar amb exactitud el seu destí a l'interior de la ultraestructura cel·lular amb la mínima pertorbació. Amb aquest objectiu, els investigadors han correlacionat en la mateixa cèl·lula, per primera vegada, dues tècniques d'imatge 3D de raigs-X amb una resolució de desenes de nanòmetres: Crio-tomografia de raigs-X tous, en la línia de llum MISTRAL de l’ALBA, i la crio-tomografia de fluorescència de raigs-X, en la línia de llum ID16A de l'ESRF. Aquestes tècniques ajuden a dilucidar l'arquitectura 3D de la cèl·lula completa i a revelar la localització intracel·lular de diferents elements atòmics, respectivament.
Gràcies a aquest estudi, publicat recentment en l'edició internacional de la revista Angewandte Chemie, l'equip ha descobert que el mecanisme d'acció d'aquesta nova família d'agents anticancerígens basat en iridi és radicalment diferent del cisplatí, la qual cosa és crucial per evitar la resistència adquirida a aquest medicament.
La Dra. Pizarro explica: "Hem estat capaços d'observar el nostre compost d'iridi - usant crio-tècniques avançades de llum de sincrotró - en cèl·lules crio-preservades de càncer de mama amb resolució en la nano-escala. Això implica que hem estat capaços de localitzar l’iridi al mitocondri cel·lular, i el més important, exclusivament al mitocondri cel·lular". Això és rellevant, ja que aquesta exclusivitat ajudaria a minimitzar els devastadors efectes secundaris que la quimioteràpia causa en pacients de càncer. D'altra banda, els mitocondris són importants orgànuls que orquestren el destí de la cèl·lula, ja que són determinants clau en la inducció de la mort cel·lular regulada.
El Dr. Javier Conesa, investigador clau en aquest projecte que treballava a la línia MISTRAL d'ALBA quan es va dur a terme la investigació, afegeix: "Hem estat capaços de quantificar específicament iridi dins del mitocondri, cosa que és tan important com única, ja que no és possible fer-ho amb marcadors fluorescents ni amb experiments en poblacions cel·lulars. També és important que la detecció s'hagi realitzat amb la cèl·lula sencera, sense seccionar, la qual cosa ha permès resoldre el context cel·lular complet i en condicions de criogènia, el que implica que l'estructura cel·lular i la composició química és molt propera a les condicions natives. Aquesta nova tecnologia correlativa 3D es pot aplicar, a més, a altres problemes biològics amb el que esperem poder estudiar altres compostos i elements d'interès".
Pizarro afegeix: "Aquests compostos d'iridi tenen el potencial de ser extremadament efectius contra el càncer, però a menys que comprenguem totalment el seu viatge dins de la cèl·lula tumoral, no tenen futur com a medicaments en clínica. Entendre això, no només ajudarà a l'aparició de fàrmacs totalment innovadors, sinó que ens proveirà de noves eines per intervenir processos relacionats amb la progressió del càncer i altres trastorns cel·lulars. És un llarg camí i aquest treball representa el primer pas."
El Dr. Javier Conesa s'ha unit recentment al Centre Nacional de Biotecnologia, després de dos anys d'investigació postdoctoral al sincrotró ALBA, per implementar una plataforma de crio-microscòpia correlativa.
La Dra. Ana Pizarro és investigadora Ramón y Cajal a IMDEA Nanociència, on estudia com molècules basades en metalls poden modular la maquinària de la cèl·lula cancerosa.
Enllaç a la notícia de IMDEA Nanociencia: https://www.imdeananociencia.org/home-en/news/item/nanoimaging-the-intracellular-space-to-aid-drug-development
Amb la col·laboració de la Fundació Espanyola per a la Ciència i la Tecnologia. El Sincrotró ALBA forma part de la xarxa d'Unitats de Cultura Científica i de la Innovació (UCC+i) de la Fundació Espanyola per a la Ciència i la Tecnologia (FECYT) i ha rebut suport a través del projecte FCT-20-15798.