Sincrotrón ALBA
Los metalofármacos basados en iridio están emergiendo como nuevas herramientas para destruir células cancerosas desajustando el balance redox intracelular. Científicos del Sincrotrón ALBA, IMDEA Nanociencia, ESRF y CNB-CSIC, han correlacionado en la misma célula, por primera vez, dos técnicas de imagen 3D de rayos-X para observar en acción un agente anticancerígeno en el nano-espacio intracelular de una célula crio-preservada.

Datos reales donde se muestra una sección 3D de una célula de cáncer de mama criopreservada. La paleta de colores que varía del malva al amarillo indica la densidad de iridio y las mitocondrias se muestra como una malla amarilla. El iridio se observa exclusivamente en el interior de las mitocondrias. También están presentes otros orgánulos: el núcleo en azul, vesículas densas en rojo, gotas lipídicas en verde y vacuolas en blanco.
Los quimioterapéuticos son fundamentales en la clínica para luchar contra la mayoría de cánceres, y los nuevos fármacos ofrecen la posibilidad de facilitar interacciones intracelulares nuevas y singulares que modulen la maquinaria celular para así destruir la célula cancerosa. De la misma manera, son necesarias nuevas herramientas que hagan posible la localización y cuantificación de tales moléculas en el nano-espacio intracelular para poder entender por completo su acción terapéutica.
Investigadores de IMDEA Nanociencia, el Sincrotrón ALBA, el Sincrotrón Europeo de Grenoble (ESRF) y el Centro Nacional de Biotecnología (CNB) han desarrollado una nueva familia de candidatos a fármaco de órgano-iridio cien veces más activos que el medicamento cisplatino, utilizado actualmente en la clínica.
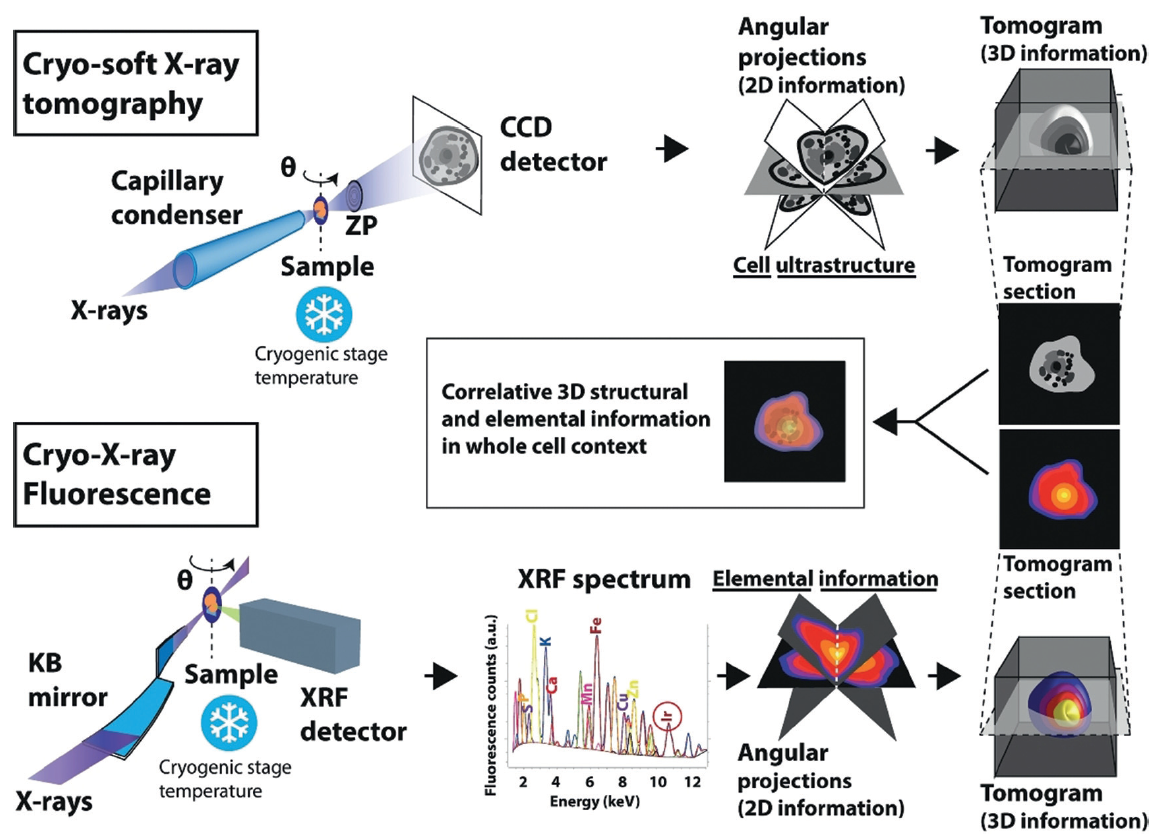
Para entender el potencial terapéutico de un compuesto, es crucial localizar con exactitud su destino en el interior de la ultraestructura celular con la mínima perturbación. Con este objetivo, los investigadores han correlacionado en la misma célula, por primera vez, dos técnicas de imagen 3D de rayos-X con una resolución de decenas de nanómetros: Crio-tomografía de rayos-X blandos, en la línea de luz MISTRAL de ALBA, y crio-tromografía de fluorescencia de rayos-X, en la línea de luz ID16A del ESRF. Estas técnicas ayudan a dilucidar la arquitectura 3D de la célula completa y a revelar la localización intracelular de diferentes elementos atómicos, respectivamente.
Gracias a este estudio, publicado recientemente en la edición internacional de la revista Angewandte Chemie, el equipo ha descubierto que el mecanismo de acción de esta nueva familia de agentes anticancerígenos basado en iridio es radicalmente diferente del cisplatino, lo cual es crucial para evitar la resistencia adquirida a dicho medicamento.
La Dra. Pizarro explica: “Hemos sido capaces de observar nuestro compuesto de iridio – usando crio-técnicas avanzadas de luz de sincrotrón – en células crio-preservadas de cáncer de mama con resolución en la nano-escala. Esto implica que hemos sido capaces de localizar el iridio en la mitocondria celular, y lo más importante, exclusivamente en la mitocondria celular”. Esto es relevante puesto que esta exclusividad ayudaría a minimizar los devastadores efectos secundarios que la quimioterapia causa en pacientes de cáncer. Por otro lado, las mitocondrias son importantes orgánulos que orquestan el destino de la célula, ya que son determinantes clave en la inducción de la muerte celular regulada.
El Dr. Javier Conesa, investigador clave en este proyecto que trabajaba en la línea MISTRAL de ALBA cuando se llevó a cabo la investigación, añade: “Hemos sido capaces de cuantificar específicamente iridio dentro de la mitocondria, lo cual es tan importante como único, ya que no es posible hacerlo con marcadores fluorescentes ni con experimentos en poblaciones celulares. También es importante que la detección se haya realizado con la célula entera, sin seccionar, lo cual ha permitido resolver el contexto celular completo y en condiciones de criogenia, lo que implica que la estructura celular y la composición química es muy cercana a las condiciones nativas. Esta nueva tecnología correlativa 3D se puede aplicar, además, a otros problemas biológicos con lo que esperamos poder estudiar otros compuestos y elementos de interés”.
Pizarro añade: “Estos compuestos de iridio tienen el potencial de ser extremadamente efectivos contra el cáncer, pero a menos que comprendamos totalmente su viaje dentro de la célula tumoral, no tienen futuro como medicamentos en clínica. Entender esto, no sólo ayudará a la aparición de fármacos totalmente innovadores, sino que nos proveerá de nuevas herramientas para intervenir procesos relacionados con la progresión del cáncer y otros trastornos celulares. Es un largo camino y este trabajo representa el primer paso.”
El Dr. Javier Conesa se ha unido recientemente al Centro Nacional de Biotecnología, tras dos años de investigación postdoctoral en el sincrotrón ALBA, para implementar una plataforma de crio-microscopía correlativa.
La Dra. Ana Pizarro es investigadora Ramón y Cajal en IMDEA Nanociencia, donde estudia cómo moléculas basadas en metales pueden modular la maquinaria de la célula cancerosa.
Enlace a la noticia de IMDEA Nanociencia: https://www.imdeananociencia.org/es/imdea-nanociencia/noticias/item/nanoimaging-the-intracellular-space-to-aid-drug-development
Con el apoyo de la Fundación Española para la Ciencia y la Tecnología. El Sincrotrón ALBA forma parte de la red de Unidades de Cultura Científica y de la Innovación (UCC+i) de la Fundación Española para la Ciencia y la Tecnología (FECYT) y ha recibido apoyo a través del proyecto FCT-20-15798.