¿Quieres estar al día? Suscríbete a nuestra newsletter. ¡1 E-mail cada 2 Meses! |
 |
Cerdanyola del Vallès, 8 de noviembre de 2021. Una colaboración entre el estudiante de doctorado Johannes Groen y la investigadora Eva Pereiro, ambos del Sincrotrón ALBA, y los grupos de Aitziber L. Cortajarena (CIC BiomaGUNE, San Sebastián) y de Ana V. Villar (IBBTEC, Santander) ha visualizado por primera vez en 3D la localización exacta de un fármaco basado en la ingeniería de nanomateriales y cuál es su comportamiento en células enteras. Este fármaco es un híbrido terapéutico entre una proteína y un nanomaterial específicamente diseñado para inhibir la sobreproducción de colágeno después de un episodio de fibrosis miocárdica.
Mediante un nuevo enfoque, el grupo de investigación combinó la luz fluorescente correlativa tridimensional y la tomografía de rayos X en condiciones criogénicas para localizar, por primera vez, el nanomaterial y obtener información en alta resolución de los cambios morfológicos de las células después del tratamiento, demostrando así las propiedades antifibróticas del fármaco.
En primer lugar, la localización intracelular permite entender qué posibles rutas se usan para entrar en la célula, en segundo lugar, cómo la célula hace frente a un agente específico y, por último, cuáles son los efectos inducidos por el tratamiento en la morfología estructural de las células.
Los resultados obtenidos en este estudio allanan el camino para la introducción de fármacos basados en nanomateriales y la nanomedicina en la clínica, ya que refuerzan la utilidad de las técnicas de imagen para evaluar la estructura celular tras la aplicación de tratamientos específicos.
Combinación de técnicas y líneas de luz
Las muestras se prepararon en el Sincrotrón ALBA y viajaron a la línea de luz B24 del Diamond Light Source (Reino Unido) para poder adquirir datos 3D de fluorescencia mediante su microscopio de iluminación estructurada tridimensional en condiciones criogénicas (cryo-3D-SIM). A continuación, en la línea de luz MISTRAL de ALBA, se realizó una tomografía de rayos X blandos también en condiciones criogénicas (cryo-SXT) que permitió estudiar las células enteras sin necesidad de teñir o manipular las muestras.
Además, el hecho de que todo el proceso se llevara a cabo en condiciones criogénicas maximizó la eficiencia al mantener tanto la integridad como la calidad de la muestra entre ambos experimentos, lo que fue crucial para poder localizar por primera vez un híbrido entre una proteína y un nanomaterial en células enteras.
El cryo-3D-SIM confirmó la presencia del agente terapéutico en las células tratadas, detectándolo a través de su señal fluorescente, mientras que la cryo-SXT reveló el entorno ultraestructural y la localización subcelular del nanomaterial con una alta correlación espacial.
Actualmente, la línea de luz MISTRAL está en proceso de obtener su propio sistema cryo-3D-SIM, que permitirá a futuros usuarios realizar todo el procedimiento experimental en el Sincrotrón ALBA.
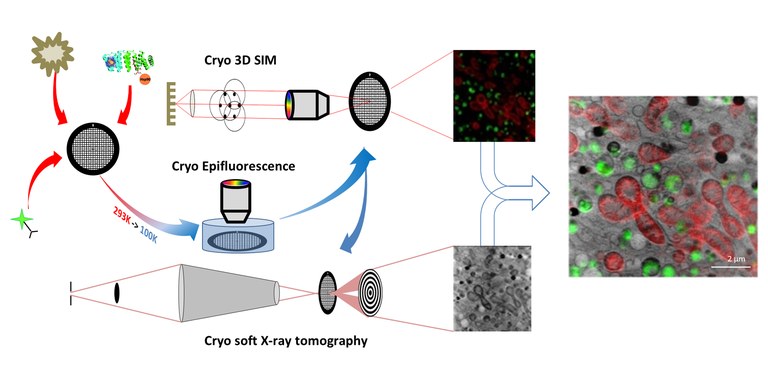
Esquema de la metodología utilizada en la investigación: luz fluorescente correlativa tridimensional (cryo-3D-SIM) y de tomografía de rayos X blandos (cryo-SXT) en condiciones criogénicas.
Fibrosis cardíaca
La fibrosis cardíaca es una afección médica que influye negativamente en la progresión de muchas enfermedades del corazón y afecta a millones de personas en todo el mundo. Esta fomenta el aumento patológico de la deposición de colágeno en el lugar de la lesión y la producción de una cicatriz, que puede dar lugar a la interrupción de las funciones de los tejidos en los peores casos.
Las causas más comunes de la fibrosis cardíaca son la isquemia, los infartos, las cardiopatías, la hipertensión y la miocarditis, las cuales requieren un seguimiento tanto a corto como a largo plazo debido a la disfunción de la bomba y la rigidez del miocardio. Estas patologías están estrechamente relacionadas con una dieta o estilo de vida poco saludables, la edad avanzada o el estrés, entre otros.
No existe ningún tratamiento preventivo o curativo para la fibrosis cardíaca, aunque algunos agentes terapéuticos prescritos para otras enfermedades cardiovasculares han mostrado ejercer un efecto beneficioso sobre ella.
En la mayoría de casos, solo es posible reducir la fibrosis miocárdica una vez que se ha aliviado la enfermedad cardiovascular subyacente, principalmente con cirugía invasiva que pone en peligro la vida del enfermo. Reducir la fibrosis podría salvar vidas al mejorar el pronóstico de los pacientes con patologías cardiovasculares.
Referencia: Johannes Groen, Ana Palanca, Antonio Aires, Javi Conesa, David Maestro, Stefan Rehbein, Maria Harkiolaki, Ana Victoria Villar, Aitziber L. Cortajarena and Eva Pereiro. Correlative 3D cryo X-ray imaging reveals intracellular location and effect of designed antifibrotic protein-nanomaterial hybrids. Chemical Science (2021). DOI: https://doi.org/10.1039/D1SC04183E

El estudiante de doctorado Johannes Groen en la línea de luz MISTRAL del Sincrotrón ALBA.
Con la colaboración de la Fundación Española para la Ciencia y la Tecnología. El Sincrotrón ALBA forma parte de la red de Unidades de Cultura Científica y de la Innovación (UCC+i) de la Fundación Española para la Ciencia y la Tecnología (FECYT) y ha recibido apoyo a través del proyecto FCT-20-15798.





