Els dominis SH3 es troben en nombroses proteïnes, en diferents quantitats i combinacions. Aquests dominis SH3 estan relacionats amb la desregulació de les vies de senyalització durant el desenvolupament del càncer i també s'associen amb altres patologies com la SIDA, l'osteoporosi i d’altres processos inflamatoris. Resoldre aquestes estructures a nivell atòmic permet una anàlisi detallada de la seva funció i característiques.
La línia de llum BL13-XALOC, dedicada a la cristal·lografia macromolecular, ha ajudat els professors Bacarizo i Cámara-Artigas a mesurar els cristalls d'aquestes estructures a resolució atòmica (0.98 Å). Per recopilar les dades mitjançant difracció de raigs X es va utilitzar el detector PILATUS.
Aquestes estructures han estat dipositades al Banc de dades de Proteïnes (PDB, a les seves sigles en anglès) i la recerca ha estat publicada a Acta Crystallographica Section D (Atomic resolution structures of the c-Src SH3 domain in complex with two high-affinity peptides from classes I and II. Julio Bacarizo and Ana Camara-Artigas, Acta Cryst. (2013). D69, 756–766; doi:10.1107/S0907444913001522).
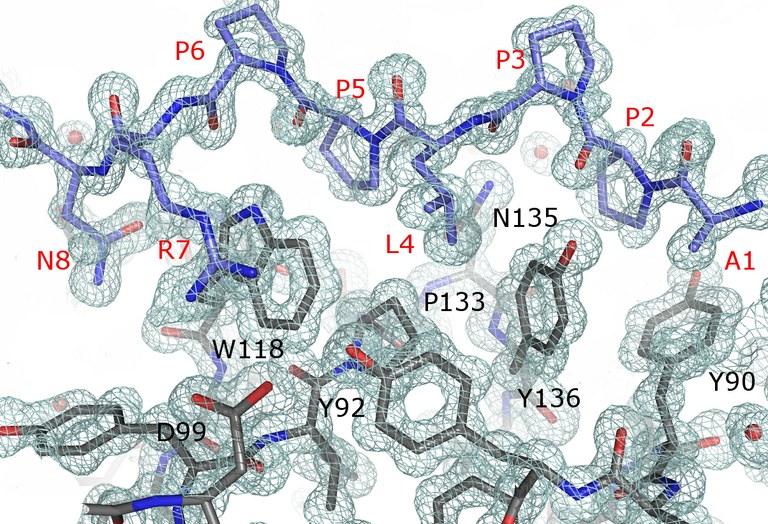
Figura 1. La imatge mostra el mapa de densitat electrònica 2Fo-Fc a 1.5 σ per al pèptid APP12 (en blau, etiqueta en vermell) i els residus del centre d'unió de la proteïna Thr98Asp mutant del domini c-Src-SH3 (en gris, etiqueta en negre).




